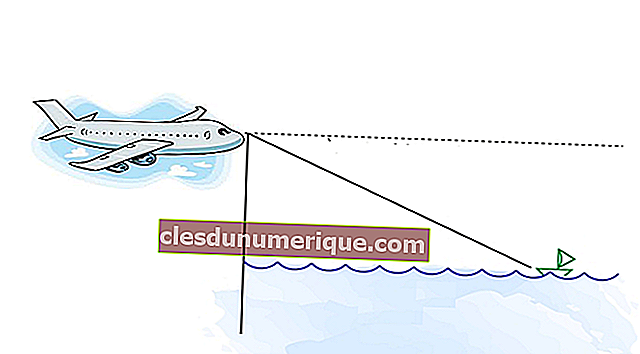
ผู้ขายน้ำแข็งหมุนจะเติมเกลือแกงลงในก้อนน้ำแข็งเสมอเมื่อทำน้ำแข็งม้วน คุณรู้ไหมว่าทำไมถึงทำเช่นนี้? ตรวจสอบการเติมเกลือมีจุดมุ่งหมายเพื่อให้ก้อนน้ำแข็งไม่ละลายเร็วเนื่องจากการทำน้ำแข็งหมุนต้องใช้อุณหภูมิที่เย็นในช่วงเวลาหนึ่ง เหตุการณ์นี้สามารถอธิบายได้ในแนวคิดของลักษณะการเรียงตัวกันของโซลูชัน
แล้วลักษณะการเรียงตัวของสารละลายมีความหมายอย่างไร? ลักษณะการเรียงตัวของสารละลายเป็นส่วนประกอบที่ขึ้นอยู่กับจำนวนอนุภาคของตัวถูกละลายที่มีอยู่ในปริมาณของตัวทำละลายภายใต้เงื่อนไขบางประการ ลักษณะการเรียงต่อกันนี้ไม่ได้ขึ้นอยู่กับคุณสมบัติและสถานะของอนุภาคแต่ละชนิด ตามที่ทราบกันดีว่าสารละลายประกอบด้วยตัวถูกละลายและตัวทำละลายซึ่งน้ำเป็นตัวทำละลายที่ดีที่สุดและมักใช้และรู้จักกันในชื่ออควาลีน
เมื่อสารละลายเกิดขึ้นคุณสมบัติทางเคมีของตัวถูกละลายจะไม่เปลี่ยนแปลงอย่างมาก แต่คุณสมบัติทางกายภาพจะเปลี่ยนไปอย่างมาก การเปลี่ยนแปลงคุณสมบัติทางกายภาพซึ่งเป็นสมบัติเชิงเปรียบเทียบ ได้แก่ การเพิ่มขึ้นของจุดเดือด (ΔTb) การลดลงของความดันไอ (ΔP) ความดันออสโมติก (π) และจุดเยือกแข็งที่ลดลง (ΔTf)
ความดันไอลดลง
ถ้าตัวถูกละลายไม่ระเหย (ไม่ระเหยไม่สามารถวัดความดันไอได้) ความดันไอของสารละลายจะต่ำกว่าความดันไอของตัวทำละลายระเหยบริสุทธิ์เสมอ สูตรนี้สามารถแสดงได้:
ΔP = P0 - หน้า
ΔP = X t x P0
P = P0 x X n
ข้อมูล :
ΔP = ความดันไอลดลง (atm)
P0 = ความดันไออิ่มตัวของตัวทำละลายบริสุทธิ์ (atm)
P = ความดันไออิ่มตัวของสารละลาย (atm)
X t = mo เศษของตัวถูกละลาย
X p = ตัวทำละลายโมลเศษส่วน
จุดเดือดเพิ่มขึ้น
จุดเดือดคืออุณหภูมิที่ความดันไอของของเหลวจะเท่ากับความดันบรรยากาศ การเติมตัวทำละลายที่ไม่ระเหยในตัวทำละลายทำให้ความดันไอลดลง
(อ่านเพิ่มเติม: ลักษณะสำคัญของเซลล์ไฟฟ้าเคมีและอนุกรมของพวกมัน)
สารละลายที่เกิดขึ้นจะต้องได้รับความร้อนที่อุณหภูมิสูงขึ้นเพื่อให้ความดันไอเท่ากับความดันบรรยากาศ ดังนั้นจุดเดือดของสารละลายจึงสูงกว่าของตัวทำละลายบริสุทธิ์
ความแตกต่างระหว่างจุดเดือดของสารละลายและตัวทำละลายบริสุทธิ์เรียกว่าการเพิ่มขึ้นของจุดเดือด สามารถกำหนดได้ดังนี้:
ΔTb = จุดเดือดของสารละลาย - จุดเดือดของตัวทำละลาย
ΔTb = kb xm
ข้อมูล :
ΔTb = จุดเดือดของสารละลายเพิ่มขึ้น (0C)
Kb = จุดเดือดโมลาลเพิ่มขึ้นอย่างต่อเนื่อง (0C / molal)
m = molality ตัวถูกละลาย (กรัม)
จุดเยือกแข็งลดลง
จุดเยือกแข็งคืออุณหภูมิที่ของเหลวและของแข็งของสารมีความดันไอเท่ากัน การเพิ่มตัวถูกละลายลงในตัวทำละลายอาจทำให้ความดันไอลดลง เส้นโค้งอุณหภูมิความดันไอน้ำสำหรับสารละลายอยู่ต่ำกว่าเส้นโค้งสำหรับตัวทำละลายบริสุทธิ์ ดังนั้นจุดเยือกแข็งของสารละลายจึงน้อยกว่าจุดเยือกแข็งของตัวทำละลายบริสุทธิ์ โดยที่สูตรในการลดจุดเยือกแข็งคือ:
ΔTf = จุดเยือกแข็งของตัวทำละลาย - จุดเดือดของสารละลาย
ΔTf = kf xm
ข้อมูล :
ΔTf = ลดจุดเยือกแข็งของสารละลาย (0C)
Kf = ค่าคงที่ลดลงของจุดเยือกแข็งโมลาล (0C / molal)
ความดันออสโมซิส
ความดันต่ำสุดที่ป้องกันการดูดซึมเรียกว่าแรงดันออสโมติก เมื่อสารละลายสองชนิดที่แตกต่างกันถูกคั่นด้วยเมมเบรนกึ่งสังเคราะห์ (เมมเบรนที่สามารถส่งผ่านอนุภาคของตัวทำละลายเท่านั้น แต่ไม่ใช่อนุภาคของตัวถูกละลาย) ก็จะเกิดปรากฏการณ์ออสโมซิส สูตรความดันออสโมติกคือπ = M x R x T
ข้อมูล :
Π = แรงดันออสโมติก (atm)
R = ความดันแก๊ส (0.0082 atm L / mol K)
T = อุณหภูมิ (K)
M = โมลาริตี (โมลาร์)